PLoS Biology: Descubren dos proteínas esenciales para el metabolismo del corazón de los recién nacidos
Un estudio publicado en la revista PLoS Biology indica, por primera vez, que el metabolismo del corazón durante la etapa postnatal es clave en la regulación del metabolismo de todo el organismo
Investigadoras del Centro Nacional de Investigaciones Cardiovasculares (CNIC) han descubierto dos proteínas esenciales para el metabolismo cardíaco tras el nacimiento. Su importancia es “clave”, se explica en un estudio publicado en la revista PLoS Biology, ya que la alteración del metabolismo cardiaco durante esos primeros días produce daños cardíacos irreversibles y una alteración de todo el metabolismo que causa diabetes y la reducción de la capacidad termorreguladora de los animales.
Afortunadamente, las investigaciones de este estudio del CNIC muestran “que estos efectos podrían llegar a ser tratados mediante un cambio en la alimentación”, asegura la Dra. Guadalupe Sabio, directora del grupo de investigación que ha llevado a cabo estos descubrimientos.
Durante el desarrollo embrionario y los primeros días tras el nacimiento, la principal fuente energética del corazón proviene de la glucosa que se almacena en forma de glucógeno. Sin embargo, tras el nacimiento, el corazón sufre un periodo de crecimiento acelerado que hace necesario un gran aporte energético por lo que, como explica la autora principal del estudio Ayelén Santamans, el corazón tiene que ser “mucho más eficiente en la obtención de energía”.
El descubrimiento que se acaba de publicar PLoS Biology muestra que las proteínas p38γ y p38d se activan en el corazón al poco de nacer y reducen la actividad de la enzima responsable de la producción del glucógeno. Esto desencadena un cambio metabólico en el corazón, que empieza entonces a utilizar ácidos grasos para producir su energía.
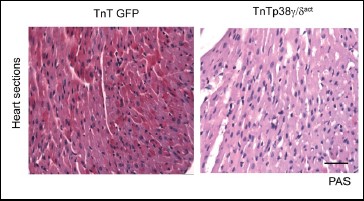
La alteración del metabolismo cardiaco durante el desarrollo postnatal provoca daños irreversibles cuyas consecuencias se hacen patentes en la etapa adulta: resistencia a la insulina, intolerancia a la glucosa y problemas para mantener la temperatura corporal.
Pero en este estudio se ha visto que, si la causa es que el corazón no obtiene la suficiente energía, los daños se puede corregir mediante un cambio en la alimentación.
Para demostrarlo, las investigadoras administraron a las madres una dieta rica en grasas.
Los resultados mostraron que los recién nacidos no presentaban ni daño cardiaco ni tampoco los síntomas de diabetes que se observan cuando estas dos proteínas descubiertas no se activan en el momento adecuado del desarrollo.
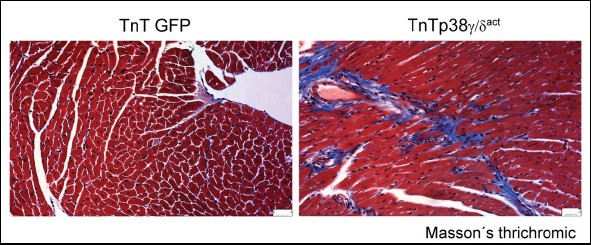
Este trabajo indica, por primera vez, que el metabolismo del corazón durante la etapa postnatal es clave en la regulación del metabolismo de todo el organismo. De hecho, explican las autoras, “lo que han descubierto es que el aumento gradual de la actividad de p38γ y p38δ está muy bien controlado y que su alteración conduce a un déficit energético perjudicial tanto para el corazón como para el metabolismo del resto del cuerpo”.
Las investigadoras consideran que tanto p38γ como p38δ podrían estar detrás de algunas de las enfermedades congénitas de origen cardiometabólico cuya causa se desconoce en la actualidad. Además, sugieren que la suplementación alimentaria podría ser un tratamiento válido para tratar este tipo de enfermedades.
En este trabajo han participado investigadores de varios grupos del CIBER de las áreas de Fragilidad y Envejecimiento Saludable (CIBERFES), Enfermedades Cardiovasculares (CIBERCV), Diabetes y Enfermedades Metabólicas asociadas (CIBERDEM) y Enfermedades Hepáticas y Digestivas (CIBEREHD). Asimismo, la investigación ha recibido apoyo de las siguientes entidades financiadoras: EFSD, Lilly European Diabetes Research Programme; Ministerio de Ciencia, Innovación y Universidades; Comunidad de Madrid; Fundación Jesús Serra; Instituto de Salud Carlos III, y Fundación “la Caixa”.











