CNIC coordina un proyecto Europeo para desarrollar un biomarcador para identificar precozmente el componente vascular del alzhéimer
El proyecto “BioClotAD”, coordinado por la investigadora del CNIC, la Dra. Marta Cortés Canteli, ha sido seleccionado por el Programa Conjunto de la UE - Investigación de Enfermedades Neurodegenerativas (JPND)
El proyecto “BioClotAD”, coordinado por la investigadora Miguel Servet del Centro Nacional de Investigaciones Cardiovasculares (CNIC), la Dra. Marta Cortés Canteli, ha sido seleccionado por el Programa Conjunto de la UE - Investigación de Enfermedades Neurodegenerativas (JPND) “Nuevos métodos y tecnologías de imagen y estimulación cerebral relacionados con enfermedades neurodegenerativas”, y recibirá una financiación de 771.430 € para los próximos tres años. El grupo de la Dra. Cortés Canteli contará con una financiación de 227.480 € para este periodo.
El Programa Conjunto de la UE - Investigación de Enfermedades Neurodegenerativas (JPND)- es la mayor iniciativa de investigación dirigida a afrontar el reto de las enfermedades neurodegenerativas. JPND tiene como objetivo aumentar la inversión coordinada entre los países participantes en la investigación destinada a encontrar causas, desarrollando curas e identificando formas adecuadas de cuidar a las personas con enfermedades neurodegenerativas (www.jpnd.eu).
El objetivo del proyecto “BioClotAD” es el desarrollo de un biomarcador de neuroimagen para identificar el estado procoagulante en la enfermedad de Alzheimer (EA).
El Consorcio está compuesto por cuatro grupos de investigación formados por expertos de instituciones europeas de vanguardia en neurociencia, bioquímica, imagen preclínica, radioquímica y enfoques traslacionales; además del CNIC, participa el grupo del Dr. Manuel Desco, del Instituto de Investigación Sanitaria del Hospital Gregorio Marañón de Madrid (IiSGM); el del Dr. Dag Sehlin, Public Health and Caring Sciences de la Universidad de Uppsala (Suecia), y el de la Dra. Susanne Kossatz, Klinikum rechts der Isar der Technischen de la Universidad de Múnich (Alemania).
La EA es la forma más común de demencia y, probablemente, la más devastadora por su impacto en la sociedad. Desgraciadamente, la mayoría de los enfoques terapéuticos han fracasado debido, en parte, a que se trata de una enfermedad multifactorial.
Por ello, los investigadores se centran ahora en el desarrollo de terapias personalizadas, compuestas por múltiples fármacos, y dirigidas a los diferentes mecanismos que contribuyen a la patología de un individuo en vez de la propuesta actual, "una diana, un tratamiento", que no ha tenido el éxito esperado hasta ahora.
Sin embargo, el éxito de este enfoque precisa el desarrollo de herramientas de diagnóstico adecuadas para identificar los diferentes factores que contribuyen al desarrollo de la enfermedad. Uno de los mecanismos que vale la pena diagnosticar y tratar es el estado procoagulante.
El objetivo del proyecto es el desarrollo de un biomarcador de neuroimagen para identificar el estado procoagulante en la enfermedad de Alzheimer
Se sabe que parte del componente vascular presente en esta enfermedad es una hipoperfusión cerebral profunda que, curiosamente, también se produce durante el deterioro cognitivo leve e, incluso, en individuos cognitivamente normales con alto riesgo de desarrollar la enfermedad de Alzheimer. Esta disminución del flujo sanguíneo cerebral se debe, en parte, a la desregulación crónica de la hemostasia presente en esta patología.
La evidencia creciente muestra que un estado protrombótico está presente en la enfermedad de Alzheimer. Dicho estado protrombótico favorece la formación y persistencia de coágulos de fibrina y contribuye al inicio y progresión de la enfermedad.
El grupo del CNIC de la Dra. Cortés Canteli ya demostró que el tratamiento a largo plazo con el inhibidor directo de trombina, dabigatrán, inhibe el depósito de fibrina cerebral y preserva la cognición, la perfusión cerebral y la función de la barrera hematoencefálica, y disminuye la neuroinflamación y el depósito de amiloide en un modelo de ratón con alzhéimer (Journal of the American College of Cardiology).
Estos resultados han abierto un campo para futuras investigaciones sobre si el uso de anticoagulantes orales ya aprobados podría tener valor terapéutico en el alzhéimer. No obstante, como parte de la multifactorialidad de este trastorno, este estado procoagulante no está presente en el 100% de los pacientes y, por lo tanto, se debe identificar aquellos que se beneficiarían de este tipo de tratamiento.
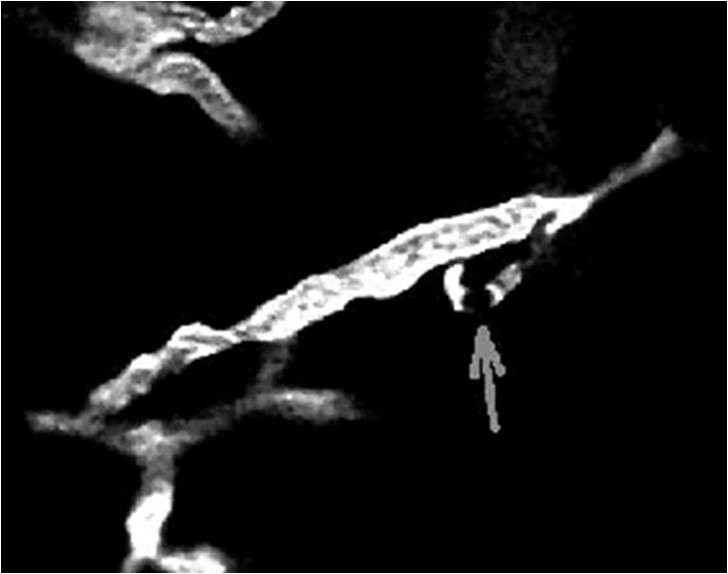
“Nuestro proyecto tiene como objetivo el desarrollo de un nuevo biomarcador de imagen no invasivo para identificar este estado procoagulante en la enfermedad de Alzheimer”, asegura la Dra. Cortés Canteli.
Para ello, añade, “usaremos modelos animales de la enfermedad de Alzheimer y enfoques de biología molecular en combinación con herramientas de imagen molecular con el objetivo de desarrollar una sonda adecuada para detectar los coágulos de fibrina en los vasos, pero también dentro del parénquima cerebral”.
La Dra. Susanne Kossatz del Hospital Universitario Klinikum rechts der Isar (TU München) en Munich, Alemania, señala que su equipo está muy emocionado de ser parte de este consorcio internacional. Este equipo investigará cómo funcionan las nuevas sondas de imágenes moleculares a nivel celular. Para ello, llevarán a cabo análisis basados en tejidos para confirmar la naturaleza selectiva y específica del enfoque de imágenes moleculares del estado protrombótico bajo investigación.
Por otro lado, los investigadores de la Universidad de Uppsala, dirigidos por el Dr. Sehlin, contribuirán al proyecto con su experiencia en la administración de medicamentos a través de la barrera hematoencefálica, que restringe el paso de moléculas entre la sangre y el cerebro. Utilizando una estrategia de "caballo de Troya" molecular, la sonda se modificará para interactuar con receptores en la barrera hematoencefálica. Esto facilitará el transporte de la sonda al parénquima cerebral, donde puede encontrar e interactuar con los coágulos de fibrina.
El grupo de Uppsala ha utilizado previamente un enfoque similar para transportar anticuerpos radiomarcados al cerebro de ratones para la obtención de imágenes PET de la patología de Alzheimer. "Vemos grandes oportunidades en este proyecto de colaboración que creemos abrirá nuevas vías para el diagnóstico y la terapia de alzhéimer", señala Sehlin.
“BioClotAD”recibirá una financiación de 771.430 € para los próximos tres años de los que 227.480 € serán para el grupo del CNIC
Dicha sonda será un biomarcador instrumental para preseleccionar aquellos pacientes con alzhéimer con un estado procoagulante que serán los adecuados para ensayos clínicos / tratamiento con antitrombóticos y para evitar la exposición de pacientes de enfermedad de Alzheimer sin estado protrombótico a los anticoagulantes.
Hay que tener en cuenta que, a pesar de que los anticoagulantes orales directos presentan bajo riesgo de hemorragia intracraneal, este existe y, por lo tanto, su uso en estos pacientes debe evaluarse cuidadosamente de forma individual, bajo el paradigma de la medicina personalizada de precisión. El biomarcador desarrollado en este proyecto jugará un papel fundamental en dicho proceso.
Para el Dr. Manuel Desco, del Instituto de Investigaciones Sanitarias Gregorio Marañón y jefe de la Unidad de Imagen Avanzada del CNIC, "el paradigma de la Medicina personalizada y de precisión va ser de aplicación en numerosos procesos patológicos, sin duda incluyendo la enfermedad de Alzheimer. La imagen molecular puede ser una herramienta de extraordinario valor en muchos aspectos de la enfermedad, incluyendo el diagnóstico, la selección de tratamientos efectivos o el establecimiento de un pronóstico preciso. En esta línea, nuestro grupo colabora en el desarrollo nuevos sondas de imagen que permitan caracterizar de modo no invasivo la fisiopatología de la enfermedad".











